Magnesium-Kontaktionen stabilisieren die makromolekulare Struktur der Transfer-RNA
In biologischen Zellen übersetzt die Transfer-RNA (tRNA) den von der Messenger-RNA (mRNA) übermittelten Bauplan von Proteinen. Neue Ergebnisse der Ultrakurzzeitspektroskopie und theoretischer Analysen zeigen, dass die komplexe gefaltete Struktur der tRNA durch Magnesium-Ionen stabilisiert wird, die sich in Kontakt mit Phosphatgruppen an ihrer Oberfläche befinden.
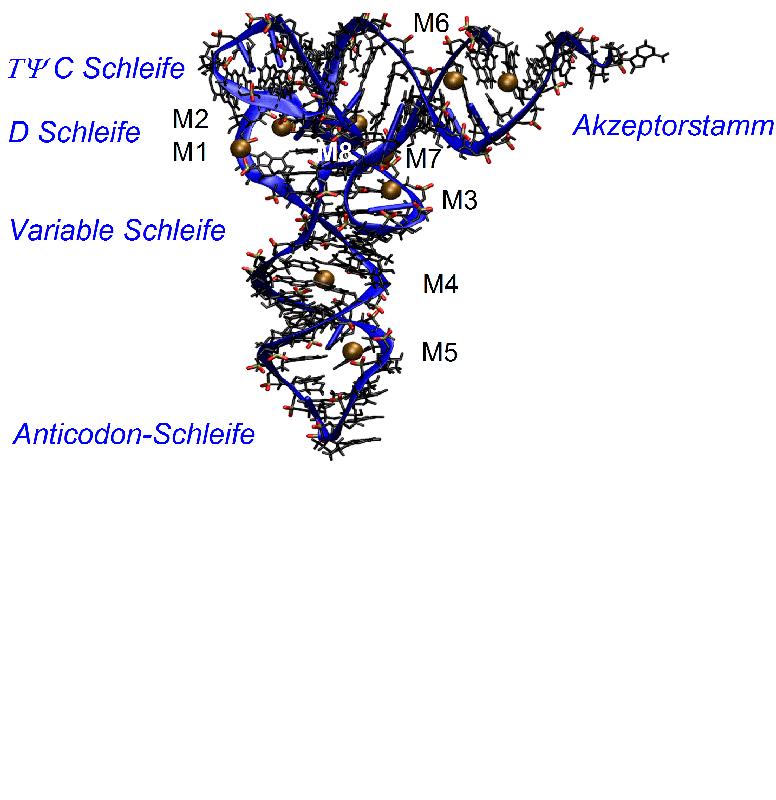
RNA-Strukturen bestehen aus langen Ketten von Nukleotiden, die sich aus einer Nukleobase, z.B. Adenin, Uracil, Cytosin oder Guanin, einer Phosphatgruppe und einem Zuckermolekül zusammensetzen. Die Phosphatgruppen weisen eine negative Ladung auf und bilden zusammen mit den Zuckereinheiten das Rückgrat des Makromoleküls, das in der Zelle als gefaltete sog. Tertiärstruktur vorliegt. Die durch Röntgenbeugung bestimmte Tertiärstruktur der tRNA von Hefe ist in Abbildung 1 gezeigt. Um diese Struktur in stabiler Form zu erhalten - eine Voraussetzung für ihre zelluläre Funktion - muss die abstoßende elektrische Kraft zwischen den negativ geladenen Phosphatgruppen durch positiv geladene Ionen und Wassermoleküle der Umgebung ausgeglichen werden. Wie das auf molekularer Ebene funktioniert, war bisher unverstanden, hinsichtlich der relevanten Anordnung von Ionen und Wassermolekülen bestehen Kontroversen in der wissenschaftlichen Literatur.
Forschern des Max-Born-Instituts ist es jetzt gelungen, Kontaktpaare von positiv geladenen Magnesium-Ionen mit den negativ geladenen Phosphatgruppen als entscheidendes Strukturelement der tRNA zu identifizieren, das die elektrostatische Energie minimiert und so die Tertiärstruktur der tRNA stabilisiert. Die in der Zeitschrift The Journal of Physical Chemistry B publizierte Studie verbindet spektroskopische Experimente mit eingehenden theoretischen Analysen der molekularen Wechselwirkungen und Dynamik.
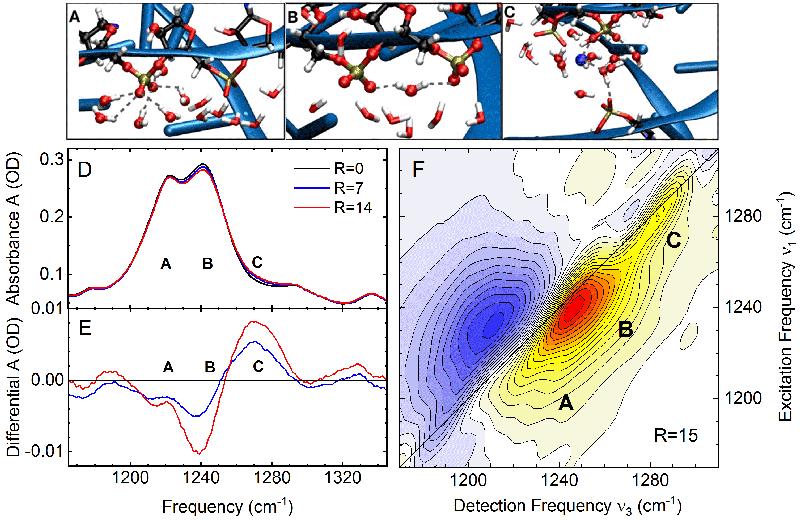
Als Sonde für die Kopplung der tRNA mit ihrer Umgebung dienen molekulare Schwingungen der Phosphatgruppen, deren Frequenz und Infrarotabsorption durch die Wechselwirkung mit Ionen und Wassermolekülen direkt beeinflusst werden. Schwingungsspektroskopie an tRNA-Proben mit unterschiedlichem Magnesiumgehalt erlaubt in Kombination mit zweidimensionaler Infrarotspektroskopie im Femtosekunden-Zeitbereich die Unterscheidung spezifischer lokaler Umgebungen, in denen Phosphatgruppen und ihre Wasserhülle koppeln (Abb. 2). Die Anwesenheit eines Magnesium-Ions in direkter Nachbarschaft einer Phosphatgruppe erhöht die entsprechende Schwingungsfrequenz und führt zum Auftreten einer neuen charakteristischen Absorptionsbande.
Messungen mit unterschiedlicher Konzentration von Magnesium-Ionen zeigen, dass eine tRNA-Struktur bis zu sechs Kontaktionenpaare ausbildet, bevorzugt an Orten, an denen benachbarte Phosphatgruppen einen geringen Abstand aufweisen und somit eine hohe negative Ladungsdichte existiert. Die Kontaktionenpaare liefern den entscheidenden Beitrag zur Absenkung der elektrostatischen Energie und damit zur Stabilisierung der Tertiärstruktur, was durch die eingehende theoretische Analyse bestätigt wird. Die Ionenpaare üben elektrische Kräfte auf Wassermoleküle der unmittelbaren Umgebung aus und orientieren sie, eine zusätzliche Stabilisierung der Struktur. Hingegen tragen bewegliche Ionen, die sich in den ersten fünf bis sechs Wasserschichten um die tRNA befinden, nur in geringerem Maß zur Stabilisierung bei.
Die Ergebnisse geben einen detaillierten quantitativen Einblick in die elektrischen Eigenschaften eines biologischen Schlüsselmoleküls. Sie unterstreichen die Bedeutung molekularer Sonden für die Aufklärung der relevanten Wechselwirkungen und die Notwendigkeit theoretischer Beschreibungen auf molekularer Ebene.
Abbildung 1. Tertiäre molekulare Struktur der Transfer-RNA von Hefe, die die Aminosäure Phenylalanin codiert. Die gefaltete Struktur besteht aus einer Abfolge von Schleifen- und Stammregionen. Das Phosphat-Zucker Rückgrat der Struktur ist als blaues Band gezeigt, mit dem die als Molekülstrukturen gezeigten Nukleobasen verbunden sind. Die Anticodon-Schleife dient zum Auslesen der durch eine Messenger-RNA bereitgestellten Information, mit der am Akzeptorstamm Proteine aus Aminosäuren hergestellt werden. An den Stellen M1 bis M8 werden bevorzugt Kontaktionenpaare gebildet.
Abbildung 2. (A-C) Aus theoretischen Simulationen ermittelte Anordnungen von Phosphatgruppen (PO4)- (Phosphor: golden, Sauerstoff: rot), Wassermolekülen H2O (Sauerstoff rot, Wasserstoff weiß) und Magnesium-Ionen (blau). Das restliche Rückgrat der RNA-Struktur ist als blaues Band gezeigt. In (A) ist die Phosphatgruppe von sechs Wassermolekülen umgeben, in (B) von einer geordneten Wasserstruktur, in (C) bildet ein Magnesium-Ion ein Kontaktpaar mit einem Sauerstoffatom der Phosphatgruppe. (D) Infrarot-Absorptionsspektrum der asymmetrischen Phosphatstreckschwingung von tRNA für verschiedene Magnesiumkonzentrationen. Die Größe R gibt das Verhältnis der Magnesiumkonzentration zur tRNA-Konzentration in der Probe an. Die in (A-C) gezeigten Geometrien führen zu den drei unterschiedlichen Absorptionsbanden A, B und C. mit zunehmender Magnesiumkonzentration nimmt die Absorption von Kontaktionenpaaren (Komponente C) zu. (E) Differenz-Infrarotspektren, die aus den Daten in Teilbild (D) gewonnen sind. Hier tritt die Absorption der Kontaktionenpaare als positive Bande hervor. (F) Zweidimensionales Infrarotspektrum von tRNA für R=15. Die Beiträge A, B und C zur Infrarotabsorption führen zu getrennten Signalkomponenten (gelb-rote Konturen). Aus der Form des Signals lässt sich die ultraschnelle Schwingungsdynamik erschließen.
Wissenschaftlicher Ansprechpartner:
Max-Born-Institut für Nichtlineare Optik und Kurzzeitspektroskopie (MBI)
Prof. Thomas Elsaesser
E-Mail elsasser@mbi-berlin.de
Tel. 030 6392 1400
Jakob Schauss
E-Mail jakob.schauss@mbi-berlin.de
Tel. 030 6392 1497
Originalpublikation:
J. Schauss, A. Kundu, B. P. Fingerhut, T. Elsaesser: Magnesium contact ions stabilize the tertiary structure of transfer RNA: electrostatics mapped by two-dimensional infrared spectra and theoretical simulations. J. Phys. Chem. B (open access).
https://doi.org/10.1021/acs.jpcb.0c08966
Ähnliche Pressemitteilungen im idw