Personalisierte Medizin - Funktionierende, künstliche Leberzellen aus Hautgewebe
Einer Forschungsgruppe aus dem Inselspital, Universitätsspital Bern, dem Universitäts-
Kinderspital Zürich – Eleonorenstiftung und der University of California San Francisco (UCSF) ist ein wichtiger Schritt zum Bau von personalisierten, künstlichen Leberzellen gelungen. Erstmals konnten technisch hergestellte Stammzellen aus Hautgewebe durch Zufügen eines Transportproteins dazu gebracht werden, sich wie normale Leberzellen zu verhalten. An diesen Zellen können nun u.a. Medikamente getestet werden.
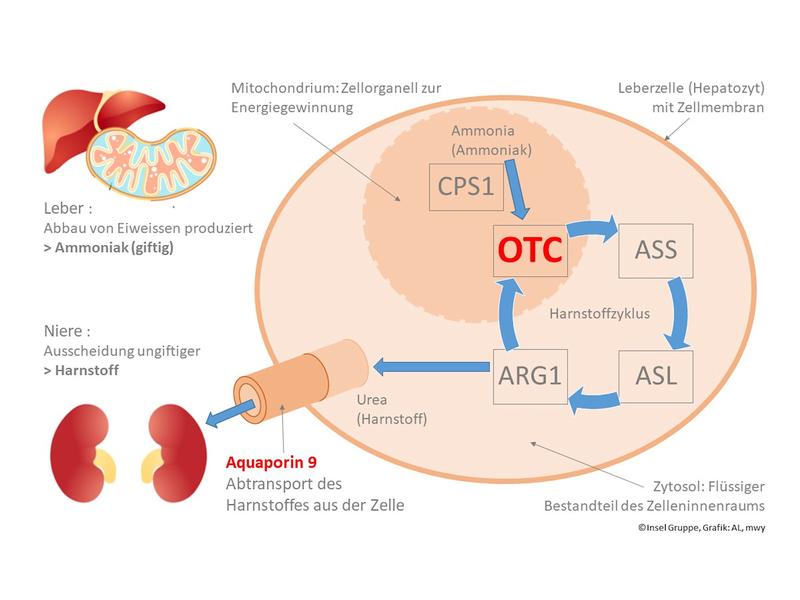
Der Harnstoffzyklus ist für die Entfernung stickstoffhaltiger Abbauprodukte aus dem Organismus verantwortlich. Fehlt in diesem Zyklus das Enzym OTC, kommt es zu Vergiftungen durch eine Anreicherung von Ammoniak. Ein OTC-Defekt ist die häufigste vererbte Krankheit im Harnstoffzyklus. Er ist mit Medikamenten bisher nicht heilbar.
Das OTC-Gen liegt auf dem Geschlechtschromosom (X-Chromosom). Das bedeutet, dass die Krankheit bei weiblichen Betroffenen in der Regel schwächer ausgeprägt ist. Bei männlichen Patienten, die ein X- und ein Y-Chromosom haben, wirkt sich ein Defekt des OTC-Gens dramatisch aus: Bei neugeborenen Jungen endet die Ammoniakvergiftung durch OTC-Mangel oft tödlich. Das Forschungsteam suchte nach Wegen, Medikamente gegen den OTC-Defekt im Labor zu testen.
Ein erstes Modell gebaut
Zuerst stellte das Forschungsteam in einem aufwendigen Verfahren künstliche Leberzellen aus dem Hautgewebe von Patientinnen und Patienten her. Das funktionierte so: Zunächst wurde Patientinnen und Patienten und einer Kontrollgruppe (gesunde Personen) eine sehr kleine Gewebeprobe der Haut entnommen. Die Proben wurden in einem technologischen Verfahren so verändert, dass sie sich wie sogenannte Stammzellen verhielten. Dieses Herstellungsverfahren wurde von Shin’Ya Yamanaka entwickelt, wofür er 2012 mit dem Medizin-Nobelpreis ausgezeichnet wurde. «Mittels induzierter Stammzellentechnologie ist es uns gelungen, künstliche Leberzellen herzustellen, die sich weitgehend wie Leberzellen von Patientinnen und Patienten verhalten» erläutert Dr. med. Alexander Lämmle, Oberarzt an der Kinderklinik und am Universitätsinstitut für Klinische Chemie am Inselspital. «Wir haben jedoch beobachtet, dass die künstlichen Leberzellen deutlich weniger Harnstoff ausscheiden als echte, gesunde Leberzellen und zwar unabhängig davon, ob sie von gesunden Kontrollen oder Harnstoffzyklus-Patientinnen und -Patienten stammen.» Den Forschenden gelang es, den Grund für dieses Verhalten zu ermitteln. Die technologisch hergestellten Stammzellen zeichneten sich durch einen vollständigen Mangel an Aquaporin 9, einem Transport-Eiweiss in der Zellmembran, aus. Grund für dieses Fehlen ist der noch unreife Charakter der künstlichen Leberzellen.
Aquaporin 9: der Schlüssel zur funktionierenden, künstlichen Leberzelle
Aquaporine organisieren den Transport von Wasser und bestimmter Stoffe durch die Zellmembran. Aquaporin 9 ist zuständig für den Transport von Harnstoff. Die Forscher haben in einem nächsten Schritt ein Verfahren entwickelt, bei dem die Bildung von Aquaporin 9 in den Stammzellen forciert wird. Dadurch ändern die technologisch hergestellten Leberzellen ihr Verhalten. Sie bauen Ammoniak zu Harnstoff ab und scheiden den Harnstoff aus – genauso, wie es gesunde Zellen tun. Damit ist die Grundlage für ein funktionierendes Testverfahren mit künstlichen Leberzellen geschaffen.
Einsatz der künstlichen Zellen: Medikamente testen
Bei einem OTC-Defekt funktionieren die komplexen OTC-Eiweissgebilde nicht richtig. Sie brauchen – wie die meisten grossen Eiweisse – Gehilfen oder Aufpasser, sogenannte Chaperone, damit sie richtig zusammengebaut werden und funktionieren können. Prof. Dr. med. Johannes Häberle vom Universitäts-Kinderspital Zürich – Eleonorenstiftung erläutert: «Die Chaperone sorgen dafür, dass die Faltung der Enzymmoleküle korrekt erfolgt und dass das Enzym korrekt für seinen Einsatz vorbereitet wird. Das neue Testmodell wird nun eingesetzt, um OTC-Chaperone zu testen und auf diese Weise mehr über den OTC-Defekt und über mögliche Therapien herauszufinden.»
Wissenschaftlicher Ansprechpartner:
Dr. med. Alexander Laemmle, Universitätsklinik für Kinderheilkunde, Inselspital, Universitätsspital Bern und Universitätsinstitut für Klinische Chemie, Universität Bern.
Prof. Dr. med. Johannes Häberle, Leitender Arzt, Leiter Stoffwechsellabor, Universitäts-Kinderspital Zürich – Eleonorenstiftung und Zurich Center for Integrative Human Physiology (ZIHP)
Prof. Holger Willenbring, M.D., Ph.D., Professor of Surgery, Eli and Edythe Broad Center of Regeneration Medicine and Stem Cell Research, Associate Director, Liver Center, University of California, San Francisco
Originalpublikation:
Laemmle, A., Poms, M., Hsu, B., Borsuk et al. (2021): Aquaporin 9 Induction in Human iPSC-derived Hepatocytes Facilitates Modeling of Ornithine Transcarbamylase Deficiency. Hepatology. Accepted Author Manuscript
DOI: https://doi.org/10.1002/hep.32247
Ähnliche Pressemitteilungen im idw