Mini-Gehirne für die Forschung der Zukunft
Organoide ahmen humane Großhirnrinde in ihrer Entwicklung und bei Krankheiten nach: „Outer Radial Glia“ (oRG)-Zellen sind Stammzellen des Nervensystems und für die Entwicklung der menschlichen Großhirnrinde von entscheidender Bedeutung. Im Labor sind sie bisher nur äußerst schwer zu kultivieren. Nun ist es einem Team von Max-Planck-Forschenden aus Berlin gelungen, Gehirnorganoide zu erzeugen, die mit diesen Stammzellen angereichert sind. Dafür haben sie bestehende Verfahren für die Mini-Organe optimiert und standardisiert.
Organoide – das sind neuartige dreidimensionale Zellkulturen, in denen Miniatur-Versionen von Leber, Gehirn oder bestimmten Krebsarten heranwachsen. Für die Forschung sind sie äußerst zukunftsträchtig, denn mit ihrer Hilfe könnten die Organentwicklung, Krankheiten und künftige Therapien in großem Maßstab erforscht werden, ohne dafür auf vollständige Organismen angewiesen zu sein. Bis ein Organoid einem echten Organ oder einem Teil davon ausreichend ähnlich ist, müssen jedoch noch viele Hürden überwunden werden.
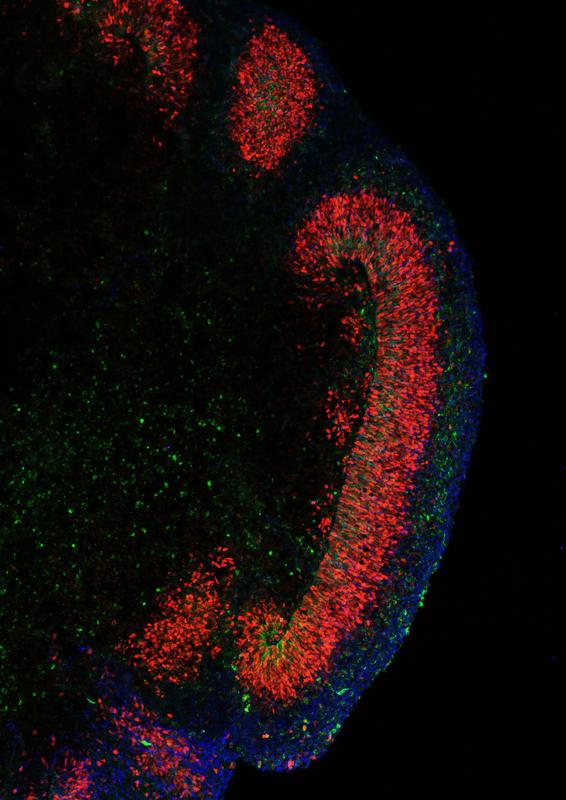
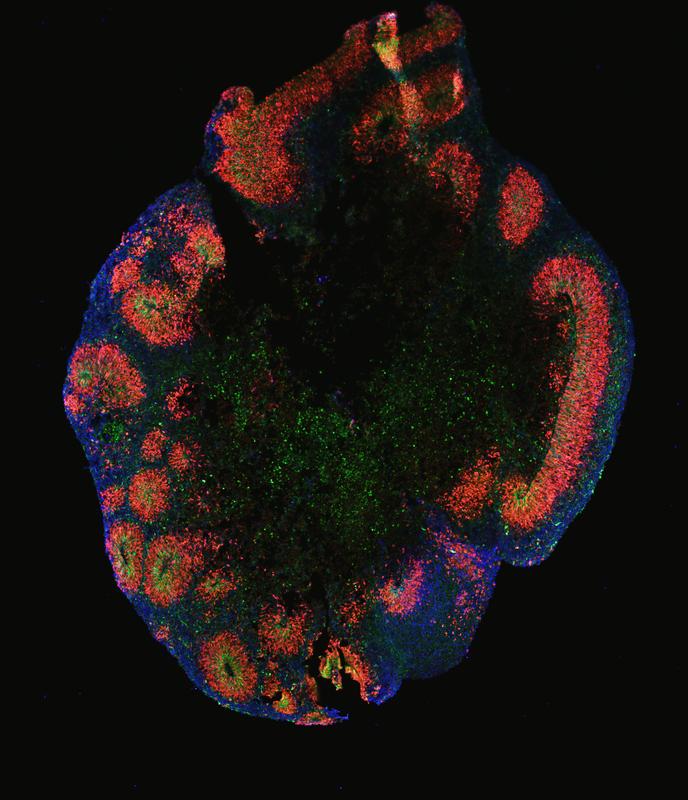
In der Fachzeitschrift Nature Cell Biology beschreiben Forschende des Max-Planck-Instituts für molekulare Genetik (MPIMG) die Kultivierung von Organoiden, die die menschliche Großhirnrinde in bislang unerreichter Qualität nachahmen. Dafür verabreichten sie Stammzellen in einem sehr frühen Stadium ihrer Entwicklung für kurze Zeit einen Cocktail aus drei chemischen Substanzen. Infolge der Behandlung bildeten die Stammzellen in den folgenden Wochen zelluläre Anhäufungen, die anatomisch die unterschiedlichen Schichten der menschlichen Hirnrinde nachahmen. Innerhalb dieser Schichten wuchsen oRG-Zellen – spezialisierte Stammzellen, die für die charakteristische Großhirnrinde von Mensch und Affe verantwortlich sind. Dies ist das erste Mal, dass diese Zellen erfolgreich in einem Zellkultursystem erzeugt, angereichert und charakterisiert wurden.
„Überraschenderweise ist es ziemlich einfach, im Labor mit auf verschiedenen Wegen Organoide vom Gehirn zu erzeugen“, sagt Yechiel Elkabetz, Forschungsgruppenleiter am MPIMG in Berlin und vormals an der Universität Tel Aviv, Israel, der die Untersuchungen leitete. „Aber es ist schwer, es gut hinzubekommen. Man muss schon zu Beginn eine sehr reine Stammzellkultur des Nervensystems schaffen und dann diese Zellen dazu bringen, neuronale Organoide mit mehreren Schichten und mit den richtigen Zelltypen an den richtigen Stellen zu bilden."
Die Baumeister des Gehirns
Neuronale Organoide können aus Gewebeproben, embryonalen Stammzellen oder sogar aus induzierten pluripotenten Stammzellen gezüchtet werden. Dabei handelt es sich um ausgewachsene Körperzellen, die so programmiert wurden, dass sie sich in das Stadium der embryonalen Stammzellen zurückverwandeln. Die bisherigen Versuche, Mini-Gehirne zu züchten waren bisher sehr uneinheitlich, sowohl was die Verfahren und das Ausgangsmaterial als auch die Organoide in ein und derselben Kulturschale betrifft.
„Neuronale Organoidkulturen sind nicht nur sehr heterogen. Die Stammzellen, aus denen die Organoide bestehen, verändern sich außerdem im Laufe der Zeit“, erklärt Sneha Arora, Forscherin in Elkabetz' Labor und eine der Erstautoren der Studie. Sie erklärt, dass es eine ganze Reihe Versuchsprotokollen gibt, die es den Zellen selbst überlassen, wie sie sich organisieren sollen – die also keine oder nur wenig Führung bekommen: „Stellen Sie sich vor, sie lassen eine Reihe Häuser bauen. Ohne genaue Anweisungen werden Ihnen die Bauleute jedes Mal ein anderes Haus hinstellen.“
Seit gut zehn Jahren suchen Labore weltweit nach den richtigen Anweisungen für die Baumeister des Gehirns. Dabei entstand eine Vielzahl an Protokollen und Verfahren – jedes Mal mit unterschiedlichen Ergebnissen. Wie ließe sich je beurteilen, welche Methode die richtige ist? Elkabetz’ Team und weitere Forschende des MPIMG wollten daher die bestehenden Techniken standardisieren und das fortschrittlichste Protokoll für Hirnorganoide entwickeln, die der menschlichen Großhirnrinde möglichst nahe kommt.
Wie auch andere Forschungsgruppen setzten sie Inhibitoren ein, chemische Wirkstoffe, die der sich entwickelnden Zelle vermitteln, in welchen Zelltyp sie sich nicht verwandeln soll. Schließlich wählt sie dann den verbleibenden, „richtigen“ Weg der Entwicklung. Die Wissenschaftler fanden heraus, dass drei verschiedene Signalwege blockiert werden mussten, um die Stammzellen dazu zu bewegen, sich einige Wochen später zu Zellen der Großhirnrinde zu entwickeln. „Erst bilden wir die besten Baumeister für unsere Organoide aus und dann bringen wir sie zum Einsatz. Sobald die Zellen ihre Anweisungen verinnerlicht haben, brauchen wir nicht mehr viel zu tun und das Organoid baut sich wie von selbst zusammen, dieses Mal korrekt“, sagt Arora.
„Die Kombination von Dual-SMAD- und WNT-Hemmung war ein Schlüsselfaktor, denn beide wurden bisher meist getrennt eingesetzt“, sagt Arora. Ihrer Meinung nach spielen das Timing und die Dosierung der Wirkstoffe eine wesentliche Rolle. „In der Anfangsphase und innerhalb von nur acht Tagen konnten wir eine sehr homogene Ausgangspopulation von Zellen erzeugen. Diese erwiesen sich als die besten Grundbausteine für das gesamte Organ.“
Ein vereinheitlichtes Protokoll
Die Forschenden erprobten zunächst parallel verschiedene Zelllinien und Verfahren. Anhand der gewonnen Erkenntnisse konnten sie schließlich konsistent Organoide der Großhirnrinde mit großer Detailtreue erzeugen. „Eine der wichtigsten Erfolge unserer Studie ist die Nachbildung der zellulären Vielfalt in jedem einzelnen Organoid“, sagt Daniel Rosebrock, Bioinformatiker in Elkabetz’ Labor und in der Abteilung für Bioinformatik am MPIMG und ein weiterer maßgeblicher Forscher des interdisziplinären Teams. „Jedes Organoid behielt die verschiedenen Zelltypen, zwischen den einzelnen Organoiden gab es aber kaum Unterschiede.“ Gewebefärbungen und die Sequenzierung von RNA aus individuellen Zellen bestätigten diese Schlussfolgerung.
„Unter all den Protokollen und Zelllinien wiesen unsere neuen Organoide das höchste Maß an kortikaler Identität auf, und zwar durchgängig“, sagt Rosebrock. Dies hat auch Auswirkungen auf Krankheitsmodelle, die Organoide verwenden: „Ob die Ausprägung einer Krankheit im Organoidmodell überhaupt etwas über die Krankheit selbst aussagt, hängt entscheidend von der Kultivierungsmethode für die Organoide ab.“
Organoidmodelle existieren für einige Erkrankungen der Gehirnentwicklung, wie zum Beispiel Mikrozephalie. Diese entsteht, weil die empfindlichen Steuerungsprozesse während der Entwicklung der Großhirnrinde gestört werden. Frühe neuronale Vorläuferzellen müssen ein Gleichgewicht finden zwischen einem ausreichenden Maß an Selbsterneuerung einerseits und der Fähigkeit zu differenzieren andererseits. Bei der Erforschung von neuronalen Krankheiten ist es daher wichtig, in den Mini-Gehirnen auch diese Prozesse nachzuahmen.
Durchbruch in der Zellkulturtechnik
Das Team wies außerdem nach, dass die Organoide oRG-Zellen entwickeln. Diese spezielle Art neuronaler Stammzellen spielt eine entscheidende Rolle bei der Gehirnentwicklung von Menschen und Affen. Sie sind für die enorm vergrößerte Hirnrinde bei Primaten verantwortlich.
„Die oRG-Zellen werden im Laufe unserer Entwicklung nach und nach zu den wichtigsten Stammzellen im Gehirn“, sagt Elkabetz. Nach einer gewissen Wachstumsphase stellen diese Zellen einen großen Teil der Stammzellen des Gehirns. „Die sich entwickelnden Gehirne von Primaten und insbesondere von Menschen sind für die Wissenschaft natürlich nur selten zugänglich. Darum sind kultivierte oRG-Zellen eine große Chance für die Entwicklungsforschung und für zukünftige therapeutische Anwendungen“, sagt der Forscher.
Nach 50 Tagen Wachstum sind die neuronalen Organoide mit dieser Art von Stammzellen angereichert. „Wir haben eine Methode entwickelt, mit der wir oRG-Zellen in der Kulturschale auf robuste und konsistente Weise erzeugen und anreichern können, wie es bisher noch nicht möglich war“, sagt Elkabetz. „Das ist ein ziemlich großer Erfolg. Wir werden endlich in der Lage sein, Modelle von Krankheiten wie Mikrozephalie herzustellen, die hinreichend aussagekräftig sind und der Realität eines echten Organs näher kommen.“
Auf diesen Erkenntnissen könne man für künftige Anwendungen in der Grundlagenforschung, bei pharmakologischen Prüfungen oder in der klinischen Praxis aufbauen, so der Wissenschaftler abschließend: „Wir liefern eine solide Grundlage für die Herstellung von neuronalen Stammzellen, aus denen später die zelluläre Vielfalt des Kortex entsteht. Wir glauben, dass dies zu Organoidmodellen für Krankheiten führen wird, die die Forschung erheblich voranbringen können.“
Wissenschaftlicher Ansprechpartner:
Dr. Yechiel Elkabetz
Gruppenleiter "Labor für humane neurale- und Gehirnstammzellen"
Max-Planck-Institut für Molekulare Genetik
+49 30 8412-1886
elkabetz@molgen.mpg.de
Daniel Rosebrock
Wissenschaftler
Max-Planck-Institut für Molekulare Genetik
+49 30 8413-1147
rosebroc@molgen.mpg.de
Originalpublikation:
Rosebrock D, Arora S, Mutukula N, Volkman R, Gralinska E, Balaskas A, Aragonés Hernández A, Buschow R, Brändl B, Müller FJ, Arndt PF, Vingron M, Elkabetz Y. Enhanced cortical neural stem cell identity through short SMAD and WNT inhibition in human cerebral organoids facilitates emergence of outer radial glial cells. Nature Cell Biology. doi:10.1038/s41556-022-00929-5
Weitere Informationen:
https://www.molgen.mpg.de/4520183/ – Web-Version dieser Mitteilung
https://www.nature.com/articles/s41556-022-00929-5 – Originalpublikation (Open Access)
Ähnliche Pressemitteilungen im idw