Publikation in Nature Chemistry: Chemiker*innen der TU Dortmund lösen molekulares Puzzle
Das Team um Prof. Guido Clever von der Fakultät für Chemie und Chemische Biologie der TU Dortmund forscht unter anderem zu den Gestaltungsprinzipien komplexer Nanostrukturen. Im renommierten Fachmagazin Nature Chemistry haben die Wissenschaftler*innen – unter ihnen auch Dr. Kai Wu und Elie Benchimol – nun eine Studie publiziert, die neue Erkenntnisse über die Synthese solcher Nanosysteme bietet und daher einen entscheidenden Fortschritt im Bereich der Supramolekularen Chemie bedeutet.
Für Forscher*innen ist es wichtig, solch komplexe molekulare Verbindungen verstehen und gezielt aufbauen zu können, um künftig Anwendungen zu entwickeln – beispielsweise selektive molekulare Rezeptoren und Katalysatoren oder maßgeschneiderte Materialien für die medizinische Diagnostik.
Bei der Untersuchung biologischer Strukturen auf atomarer Ebene fasziniert die Komplexität der Formen und Funktionen, die die Grundlage allen Lebens auf der Erde bilden. Während die Natur im Laufe von Milliarden von Jahren verflochtene Netzwerke von interagierenden molekularen Strukturen entwickelt hat, stehen synthetische Chemiker*innen immer noch vor großen Herausforderungen bei der Synthese komplexer Moleküle. Ein Ansatz ist die mehrstufige organische Synthese, die mühsame und ressourcenintensive Laborarbeit erfordert, oft über viele Jahre hinweg.
Eine andere Strategie nennt sich Selbst-Assemblierung und basiert darauf, eine Gruppe einfacher Bausteine zusammenzubringen, die sich durch schwache und dynamische Wechselwirkungen miteinander zu einem größeren Objekt verbinden. Der Verlauf des Strukturbildungsprozesses wird dann üblicherweise von grundlegenden geometrischen Faktoren kontrolliert, bis alle zufällig aufeinandertreffenden Komponenten ein stabiles Produkt gebildet haben. In diesem Prozess zerfallen fehlerhaft zusammengesetzte, instabile Teile wieder und beteiligen sich an der Bildung des stabilen Endprodukts, bis alle Bausteine verbraucht sind. Dieses Verfahren, das mit einem sich selbst lösenden Puzzle vergleichbar ist, litt bisher oft unter der begrenzten Anzahl verschiedener Bausteine, die im finalen Produkt vereint werden konnten. Wurde bislang versucht, eine größere Vielfalt und Anzahl von Komponenten einzubeziehen, um niedriger symmetrische Anordnungen zu erreichen, die den biologischen Strukturen in Bezug auf Form und Funktion näherkommen, sah man oft die Bildung statistischer Mischungen einer Vielzahl selbst-assemblierter Objekte. Das heißt: Die Bausteine konnten nicht entscheiden, welches Produkt sie bilden sollen, und das molekulare Puzzle ergab keine definierte Lösung.
Zusammenspiel organischer Bausteine mit Metallen kontrolliert
Hier setzt die Forschung der Arbeitsgruppe um Prof. Guido Clever an: Im Rahmen des vom Europäischen Forschungsrat finanzierten Projektes RAMSES hat das Team eine Reihe von Strategien entwickelt, um diese Einschränkung zu überwinden und die Wechselwirkung von unterschiedlichen Bausteinen zu kontrollieren. Dadurch wird die strukturelle und funktionale Komplexität dieser molekularen Puzzles erhöht und so auch näher an Anwendungen herangeführt. Die Gruppe hatte zuvor bereits komplexe Nanostrukturen realisiert, indem sie den Schritt von der Selbst-Assemblierung zu einer Selbst-Sortierung machte. Die dadurch erhaltenen Nanostrukturen können als spezifische Rezeptoren für Biomoleküle, einstellbare optische Werkzeuge und neue Emulgatoren für organische Lösungsmittel dienen. Die Funktionen dieser Systeme basierte jedoch zunächst auf dem Zusammenspiel zwischen nur zwei chemisch unterschiedlichen Bausteinen.
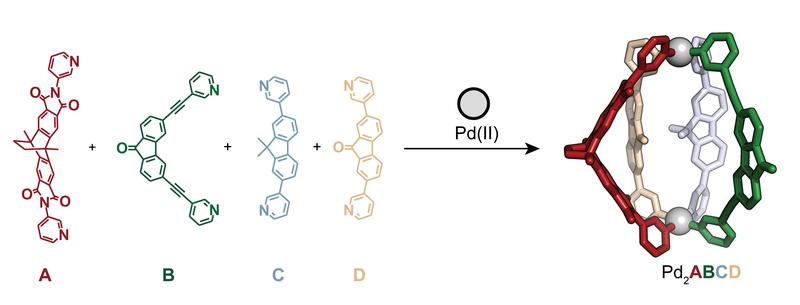
Jetzt erfolgte ein weiterer großer Schritt, indem gezeigt wurde, dass alle vier organischen Bausteine (A, B, C, D) eines nanoskopischen Käfigs, also einer molekularen Architektur mit einem inneren Hohlraum, ohne die Bildung eines statistischen Durcheinanders differenziert werden können. Bei der Mischung von A, B, C und D mit zwei Ionen des Metalls Palladium, das als molekularer Kleber wirkt, wird nur ein definiertes Produkt beobachtet, nämlich Pd2ABCD. Andere der 55 Kombinationen, die ohne Kontrolle über die Selbst-Sortierung zu erwarten gewesen wären, entstehen nicht. Der Schlüssel zu diesem Erfolg ist die Kombination mehrerer Kontrollmechanismen, darunter die sogenannte Formkomplementarität zwischen ausgewählten Bausteinen und direkte Wechselwirkungen zwischen benachbarten Einheiten im Endprodukt. Auf diese Weise konnte das Team Ordnung in ein Chaos bringen, das entstünde, wenn man das System vollständig der Entropie überlassen würde, also der natürlichen Tendenz zu wachsender Unordnung.
Die aktuelle Publikation in Nature Chemistry wurde von der Fachcommunity bereits durch zwei weitere Highlights gewürdigt: Durch eine Empfehlung in ChemistryViews, dem gemeinsamen Wissenschaftsmagazin von 16 europäischen Chemiegesellschaften, sowie durch einen Preview Artikel im Fachmagazin Chem, in dem Wissenschaftler der Universität Otago, Neuseeland, die Publikation von Prof. Clever und seinem Team im Hinblick auf den Fortschritt im Gebiet der synthetischen Chemie besprechen.
Wissenschaftlicher Ansprechpartner:
Prof. Dr. Guido Clever
Technische Universität Dortmund
Fakultät für Chemie und Chemische Biologie
E-Mail: guido.clever@tu-dortmund.de
Tel.: +49 231 755 8677
Originalpublikation:
https://www.nature.com/articles/s41557-023-01415-7
Weitere Informationen:
https://www.sciencedirect.com/science/article/pii/S2451929424000196?via%3Dihub
Die semantisch ähnlichsten Pressemitteilungen im idw