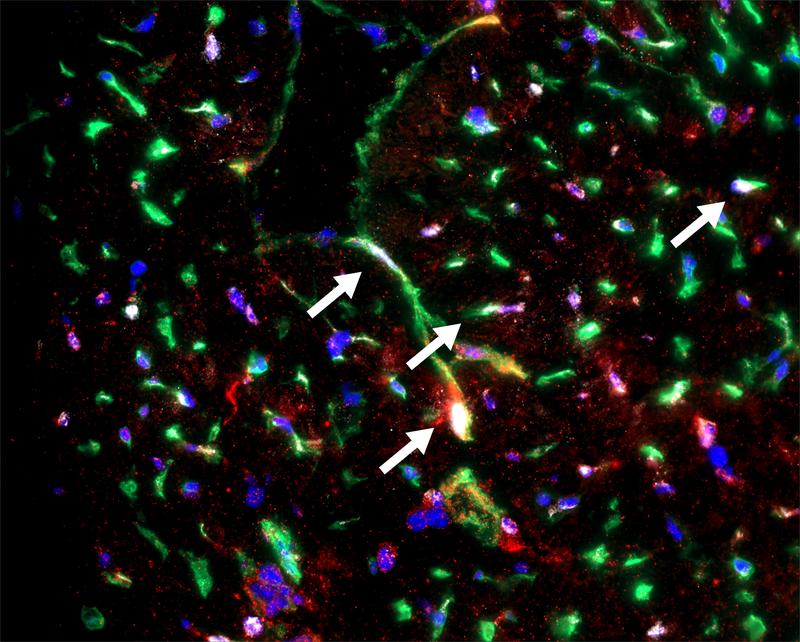
Kleine Zellpopulation mit großer Wirkung
Endothelzellen kleinster Gefäße erweisen sich als vielversprechendes therapeutisches Ziel bei Organfibrose
Krankhafte Ablagerung von Bindegewebe (Fibrose) ist eine Begleiterscheinung vieler chronischer Erkrankungen, die mittel- bis langfristig zum Organversagen führen kann. Wissenschaftler am European Center for Angioscience (ECAS) der Medizinischen Fakultät Mannheim der Universität Heidelberg und dem Deutschen Zentrum für Herz-Kreislauf-Forschung (DZHK) haben in einer Subpopulation von Endothelzellen im Transkriptionsfaktor SOX9 einen Regulator der Fibrose ausmachen können.
Die Arbeit ist nun in der renommierten wissenschaftlichen Zeitschrift Science Translational Medicine veröffentlicht worden. Die das Innere der kleinsten Blutgefäße (Kapillaren) auskleidenden Endothelzellen könnten damit ein vielversprechendes Ziel sein, um fibrotischen Erkrankungen und Organversagen entgegenzuwirken.
Bei der Fibrosierung kommt es durch eine krankhafte Vermehrung und Aktivierung von Bindegewebszellen zu einer überschießenden Ablagerung von Bindegewebe. Eine Fibrose kann je nach Erkrankung in nahezu allen Organen vorkommen. Je mehr das funktionale Organgewebe durch Bindegewebe verdrängt wird, umso stärker wird die Funktion des betroffenen Organs eingeschränkt.
Dass sogenannte Fibroblasten, teilungsaktive Zellen des Bindegewebes, im Mittelpunkt der Fibrose stehen, ist unumstritten. Doch wie kommt es dazu, dass Fibroblasten im Verlauf vieler chronischer Krankheiten dazu angeregt werden, Bindegewebe zu produzieren – und wie lässt sich dies verhindern?
Für Ihre Untersuchungen nutzten die Forscher um Dr. Felix Trogisch und Professor Dr. Jörg Heineke von der Abteilung Kardiovaskuläre Physiologie am ECAS (Leitung: Prof. Heineke) Mausmodelle fibrotischer Erkrankungen. Dabei stellten sie fest, dass in den kapillären Endothelzellen fibrotischer Mausorgane die Expression des Transkriptionsfaktors SOX9 hochreguliert ist.
Um herauszufinden, wie wichtig die Rolle von SOX9 bei der krankhaften Fibrosierung ist, sollte untersucht werden, ob eine „Abschaltung“ von SOX9 im Endothel der Kapillaren die Erkrankung günstig beeinflusst.
In der Tat schützte das genetische Ausschalten von SOX9 im Endothel bei Mäusen mit Herzschwäche, Leber- oder Lungenerkrankung vor der Entwicklung einer Fibrose, und die Organfunktion blieb erhalten. Sogar wenn die Erkrankung bereits fortgeschritten war, konnte sie durch das Ausschalten von SOX9 gestoppt werden.
Weitere Untersuchungen mittels Massen- und Einzelzell-RNA-Sequenzierung brachte Licht in den Mechanismus, über den SOX9 agiert: Der Transkriptionsfaktor bringt die Endothelzellen dazu, sowohl selbst Bindegewebe zu produzieren, als auch durch vermehrte Produktion von Botenstoffen benachbarte Fibroblasten zur Migration und Ablagerung von Matrix zu aktivieren.
„Unsere Ergebnisse zeigen, dass die kleinsten Gefäßzellen tatsächlich eine wichtige Rolle bei der Entwicklung der Organ-Fibrose spielen, und somit therapeutisch gezielt verändert werden könnten, um dem krankhaften Bindegewebe entgegenzuwirken und die Organfunktion zu erhalten“, erläutert Jörg Heineke.
„Für eine therapeutische Hemmung von endothelialem SOX9 ist es möglicherweise vorteilhaft, dass SOX9 bei der Fibrosierung nur in einer zahlenmäßig kleinen Population von Endothelzellen angeschaltet wird. Es ist eine kleine Zellpopulation, die jedoch leider eine weitreichende ungünstige Wirkung hat. Wir arbeiten nun daran, Methoden zu entwickeln, um diese Zellen therapeutisch gezielt zu erreichen und SOX9 dort zu hemmen“, ergänzt Felix Trogisch.
Die Arbeit ist eine weitere Bestätigung für die große Bedeutung der „Angioscience“ – die gezielte Erforschung des Blutgefäßsystems als Regulator der Organfunktion und als Auslöser für verschiedenste Erkrankungen – am Mannheimer European Center for Angioscience und am dort angesiedelten Sonderforschungsbereich 1366 „Vascular Control of Organ Function“.
Originalpublikation:
Trogisch et al.
Endothelial cells drive organ fibrosis and dysfunction by inducing the transcription factor SOX9
Science Translational Medicine, Vol 16, Issue 736
https://doi.org/10.1126/scitranslmed.abq4581
Ähnliche Pressemitteilungen im idw