Lebervernarbung: Neue Erkenntnisse könnten die Behandlung von Leberfibrose verbessern
Wird die Leber wiederholt geschädigt, etwa durch eine Virus-Hepatitis oder durch Alkoholkonsum, bildet sich durch einen komplizierten molekularen Prozess eine Lebervernarbung (eine sog. Leberfibrose). ForscherInnen am CeMM und der MedUni Wien gelang es nun in einer neuen Studie, diesen Prozess besser zu verstehen, indem sie die Genaktivitäten in verschiedenen Stadien der Erkrankung untersuchten. Ihre Ergebnisse könnten zu einer erstmaligen Therapie der Fibrose beitragen.
Die Leber ist nicht nur das größte innere Organ, sondern als Stoffwechselzentrale auch lebensnotwendig für den menschlichen Körper. Sie besitzt auch erstaunliche Selbstheilungskräfte: Selbst wenn größere Teile entfernt werden, etwa bei einer Operation, wachsen diese in gesunden Menschen rasch nach. Bei wiederholten oder chronischen Verletzungen des Lebergewebes, wie sie etwa durch massiven Alkoholkonsum oder einer Virushepatitis entstehen, versagt diese Regenerationsfähigkeit jedoch. Es kommt zu einer Vernarbung, der sogenannten Fibrose, bei der Leberzellen durch Bindegewebe ersetzt werden. Die Leber verhärtet und kann ihre Aufgaben immer schlechter ausführen – im schlimmsten Fall führt das zu einem Leberversagen.
Um den Prozess der Vernarbung besser zu verstehen hat ein Forschungsteam unter der Leitung von Thomas Reiberger, Professor für Gastroenterologie und Hepatologie an der MedUni Wien und Adjunct Principal Investigator am CeMM, die Genaktivität in zwei verschiedenen Mausmodellen untersucht, die verschiedene Schweregrade einer Lebererkrankung aufwiesen, und dabei auch bestimmte Phasen der spontanen Regression der Erkrankung erfasst. Gleichzeitig wurden wichtige Kennwerte der Erkrankungsschwere, wie der Pfortaderdruck, Blutmarker für Leberschäden oder des Ausmaßes der Lebervernarbung anhand von Lebergewebsproben aufgezeichnet. Die Ergebnisse wurden in dem Fachjournal iScience publiziert (DOI: 10.1016/j.isci.2024.109301)
Dynamische molekulare Prozesse können Leberfibrose rückgängig machen
Es zeigte sich ein sehr dynamisches Muster der Genexpression, sowohl während der Entwicklung der Fibrose als auch interessanterweise während der Rückbildung der Leberfibrose. Manche Gene wurden hochreguliert beim Voranschreiten der Erkrankung und gedrosselt während der Rückbildung, bei anderen war es genau umgekehrt; wieder andere Gene zeigten in allen Phasen eine veränderte Aktivität, was auf persistierende Langzeiteffekte von Leberschäden hindeutet. Mit Hilfe neuester bioinformatischer Methoden konnten diese genetischen Muster mit den oben beschriebenen, Erkrankungskennwerten verknüpft werden. Dabei identifizierten die Forscherinnen und Forscher genetische Treiber der Erkrankung, die als Angriffsziele Potential für die Entwicklung von zukünftigen Therapien haben.
Durch eigens entwickelte Netzwerk-Algorithmen konnten vier wichtige Gengruppen identifiziert werden, die mit der Dynamik der Fibrose, dem Pfortaderdruck, den histologischen Daten und den Blutmarkern in Verbindung gebracht werden konnten. Diese sogenannten „hub“-Gene könnten alle zu klinisch relevanten Biomarkern weiterentwickelt werden. Dies wurde in der Studie auch mit Datensätzen von Patienten mit Lebererkrankungen getestet und bestätigt. In Kollaboration mit Forschenden der Universität Strasbourg und dem Institut Universitaire de France wurden manche der „hub“-Gene auch bei Patienten, die von Hepatitis-C geheilt wurden, und dadurch auch eine zurückgebildete Lebererkrankung hatten, bestätigt.
Die vorliegende Studie enthüllt genetische Mechanismen in der Entstehung von Leberfibrose und bietet neue therapeutische Möglichkeiten, um in diese Mechanismen einzugreifen. Es bedarf weiterer Studien, um das Potential der Hub-Gene genau zu verstehen und für therapeutische Strategien einzusetzen, die sich auf die Regression der Leberfibrose fokussieren – besonders bei Patienten mit Leberzirrhose, die eine Alkoholabstinenz einhalten oder von einer Virushepatitis geheilt wurden.
Bilder im Anhang
Foto: Erstautor Oleksandr Petrenko (l) und Korrespondierender Autor Thomas Reiberger (r) © Anna Yuwen / CeMM
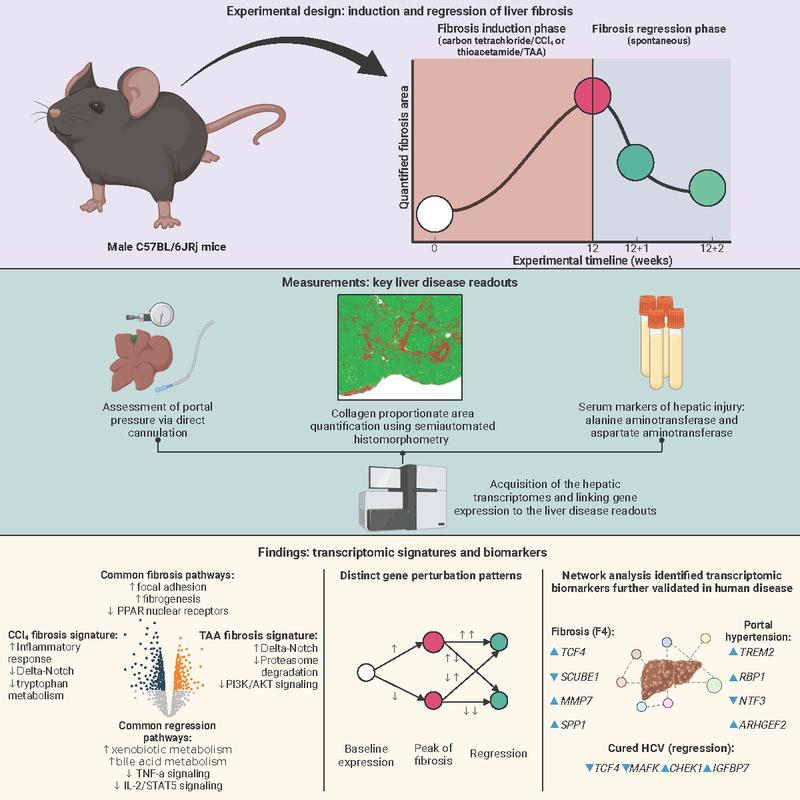
Grafik: Graphische Zusammenfassung der Studie
© iScience
Die Studie „Transcriptomic signatures of progressive and regressive liver fibrosis and portal hypertension“ erschien in der Zeitschrift iScience am 15. März 2024 . DOI: 10.1016/j.isci.2024.109301
AutorInnen: Oleksandr Petrenko, Philipp Königshofer, Ksenia Brusilovskaya, Benedikt S. Hofer, Katharina Bareiner, Benedikt Simbrunner, Frank Jühling, Thomas F. Baumert, Joachim Lupberger, Michael Trauner, Stefan G. Kauschke, Larissa Pfisterer, Eric Simon, André F. Rendeiro, Laura P.M. H. de Rooij, Philipp Schwabl, Thomas Reiberger
Förderung: Thomas Reiberger wurde für diese Studie vom Österreichischen Bundesministerium für Digitalisierung und Wirtschaftsstandort, der Nationalstiftung für Forschung, Technologie und Entwicklung, Boehringer Ingelheim und der Christian Doppler Forschungsgesellschaft unterstützt.
Das CeMM Forschungszentrum für Molekulare Medizin der Österreichischen Akademie der Wissenschaften ist eine internationale, unabhängige und interdisziplinäre Forschungseinrichtung für molekulare Medizin unter wissenschaftlicher Leitung von Giulio Superti-Furga. Das CeMM orientiert sich an den medizinischen Erfordernissen und integriert Grundlagenforschung sowie klinische Expertise, um innovative diagnostische und therapeutische Ansätze für eine Präzisionsmedizin zu entwickeln. Die Forschungsschwerpunkte sind Krebs, Entzündungen, Stoffwechsel- und Immunstörungen, sowie seltene Erkrankungen.
Das Forschungsgebäude des Institutes befindet sich am Campus der Medizinischen Universität und des Allgemeinen Krankenhauses Wien.
www.cemm.at
Die Medizinische Universität Wien (kurz: MedUni Wien) ist eine der traditionsreichsten medizinischen Ausbildungs- und Forschungsstätten Europas. Mit rund 8.000 Studierenden ist sie heute die größte medizinische Ausbildungsstätte im deutschsprachigen Raum. Mit mehr als 6.000 Mitarbeiter:innen, 30 Universitätskliniken und zwei klinischen Instituten, zwölf medizintheoretischen Zentren und zahlreichen hochspezialisierten Laboratorien zählt sie zu den bedeutendsten Spitzenforschungsinstitutionen Europas im biomedizinischen Bereich. Die MedUni Wien besitzt mit dem Josephinum auch ein medizinhistorisches Museum. www.meduniwien.ac.at
Für Rückfragen wenden Sie sich bitte an:
Stefan Bernhardt
PR & Communications Manager
CeMM
Research Center for Molecular Medicine
of the Austrian Academy of Sciences
Lazarettgasse 14, AKH BT 25.3
1090 Vienna, Austria
Phone +43-1/40160-70 056
Fax +43-1/40160-970 000
sbernhardt@cemm.at
www.cemm.at
Originalpublikation:
DOI: 10.1016/j.isci.2024.109301
Ähnliche Pressemitteilungen im idw