Die Selektivität von Katalysatoren als “Balanceakt“
Forschende der Abteilung für Anorganische Chemie des Fritz-Haber-Instituts haben aufgezeigt, wie strukturelle Veränderungen an der Oberfläche und im Inneren des Kobaltoxid-Katalysators Co3O4 dessen Selektivität bei der Herstellung industriell relevanter Chemikalien wie Aceton beeinflussen. Sie entdeckten, dass ein metastabiler, strukturell „gefangener” Zustand die höchste katalytische Aktivität zeigt – eine wichtige Erkenntnis für das Katalysatordesign.
Wichtige Aspekte
- Industriell relevante Reaktion: Die Studie beleuchtet die katalytische Oxidation von Isopropanol (2-Propanol) zu Aceton, eines Stoffs, der in Industrie und Laboren weit verbreitet ist.
- Einblicke in die Selektivität von Katalysatoren: Die Studie zeigt, wie die Struktur des Kobaltoxidkatalysators Co₃O₄ und strukturelle Umordnungsprozesse an seiner Oberfläche „während seiner Arbeit“ die katalytische Leistung beeinflussen.
- Optimierung der Katalyse: Die höchste Aktivität und Selektivität des Katalysators wird beobachtet, wenn sich der Katalysator in einem einzigartigen metastabilen, „eingeschlossenen” Strukturzustand befindet – und nicht in einer stabilen, ideal geordneten kristallinen Form.
- Katalysatordesign überdenken: Die aktuellen Erkenntnisse könnten zur Entwicklung selektiverer, effizienterer und stabilerer Katalysatoren beitragen und so Nebenprodukte, Energiekosten und Trennschritte bei der industriellen Herstellung von Chemikalien wie Aceton verringern.
Heterogene Katalyse, ein Eckpfeiler der chemischen Industire
Von der Ammoniaksynthese bis zur Kunststoffherstellung ist die heterogene Katalyse ein grundlegender Prozess in der chemischen Industrie. Der Katalysator liegt oft in fester Form vor, während andere Reagenzien flüssig oder gasförmig sind, was für die Trennung der Reaktionsprodukte am Ende ideal ist. Daher wird viel Forschung in die Entwicklung und Verfeinerung heterogener Katalysatoren investiert. Diese Studie zeigt deutlich, dass hierbei Erkenntnisse über die Prozesse auf der Katalysatoroberfläche berücksichtigt werden müssen.
Selektivität in der Katalyse
Der ideale Katalysator kann eine bestimmte, gewünschte Reaktion bevorzugt fördern, wenn mehrere Reaktionswege konkurrieren – er ist selektiv. Diese Eigenschaft, die durch das Design des Katalysators gesteuert werden kann, ist für industrielle Prozesse von entscheidender Bedeutung, da sie die Produktreinheit verbessert und Energie spart, da sie umständliche Produktabscheidungsprozesse nach der Reaktion vermeidet. Allerdings bleibt oft unklar, was genau die Selektivität auf molekularer Ebene bestimmt. Um dies zu verstehen, verwendet das Forschungsteam unseres Instituts Operando-Methoden, mit denen es die Katalysatoren „bei der Arbeit“ beobachten kann.
Ein neues Verständnis der katalytischen Oxidation
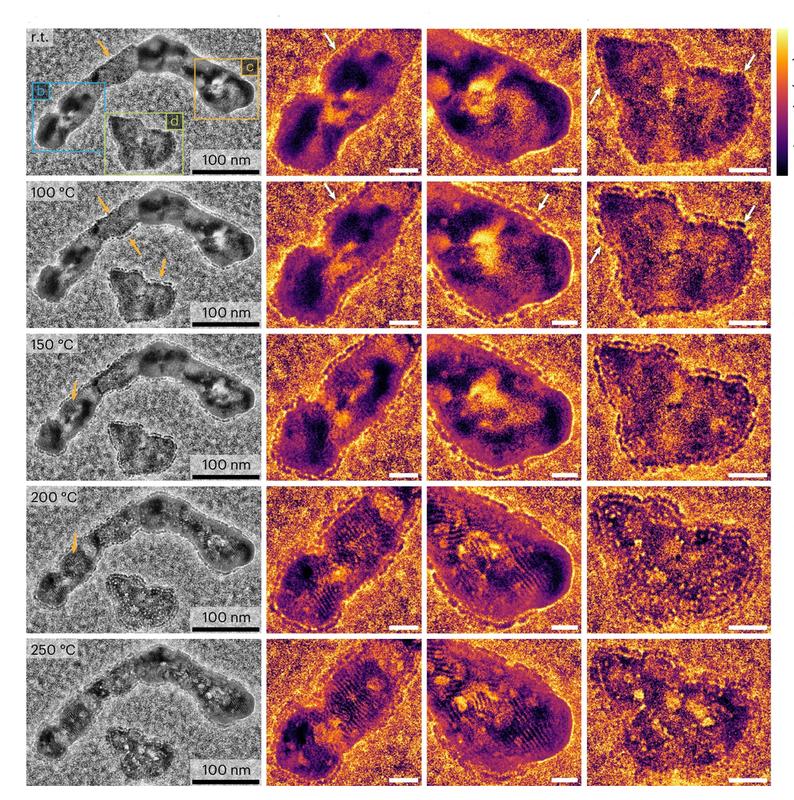
In ihrer aktuellen Studie beleuchtet das Forschungsteam einen bedeutenden heterogen katalysierten industriellen Prozess, bei dem Selektivität eine wichtige Rolle spielt: die Oxidation von Isopropanol (2-Propanol) zu Aceton unter Verwendung von Kobaltoxid (Co₃O₄) für die thermische Katalyse. Sie kombinieren Operando-Röntgenspektroskopie und Operando-Transmissionselektronenmikroskopie (TEM), um einen genaueren Einblick in die Leistung des Katalysators zu erhalten. Insbesondere interessieren sich die Forschenden dafür, wie die Katalysatorleistung durch die Prozesse beeinflusst wird, die auf der Katalysatoroberfläche und unmittelbar darunter in seinem Inneren (dem Volumenbereich) ablaufen.
Wie beeinflussen Reaktionen auf der Oberfläche des Katalysators seine Leistung?
Ein Vergleich der Katalysatoraktivität, die in einem Reaktor gemessen wurde und der operando-Informationen über die strukturellen Veränderungen während des Katalysatorbetriebs ergibt zwei Phasen der Aktivität des Katalysators: eine unterhalb und eine oberhalb von 200 °C. Bei niedrigeren Temperaturen verzerrt ein Zusammenspiel verschiedener Festkörperprozesse wie Diffusion und Defektbildung die Katalysatorstruktur, die die katalytischen Eigenschaften von Co3O4 steuert, während bei höheren Temperaturen die Kristallordnung dominiert.
Interessanterweise findet sich die ideale Kombination aus Aktivität und Selektivität des Katalysators genau bei 200 °C, nämlich an der Grenze der beiden Phasen. Man kann sich vorstellen, dass der Katalysator hier in einem Übergang zwischen zwei energetisch äquivalenten Zuständen „gefangen“ ist, wobei kleinste Änderungen der Bedingungen dazu führen können, dass das System zwischen diesen Zuständen hin- und herwechselt. Um die optimale Leistung zu erhalten, sollte man also den Katalysator in diesem Zustand zu halten. Dies kann durch die Schaffung optimaler Arbeitsbedingungen erreicht werden oder auch durch das Design des Katalysators und eine geeignete Vorbehandlung.
Bedeutung der Erkenntnisse
Die Ergebnisse der Studie stellen herkömmliches Katalysatordesign infrage. Die Studie legt nahe, dass die Suche nach einem „perfekten, stabilen“ kristallinen Katalysator suboptimal sein kann. Es wird deutlich, dass Veränderungen der Oberflächenstruktur die Aktivität und Selektivität von Oxidationskatalysatoren entscheidend beeinflussen. Die gewählte Methodik – eine Kombination aus Operando-Spektroskopie, Mikroskopie und Aktivitätsmessungen – setzt neue Maßstäbe für die Untersuchung von Katalysatoren unter realistischen Bedingungen. Sie erfasst dynamische Verhaltensweisen, die bei herkömmlichen Analysen nicht sichtbar sind.
Schließlich legt die Studie einen Paradigmawechsel in der heterogenen Katalyse nahe: Katalysatoroberflächen sollten nicht mehr nur als statisch betrachtet werden, sondern als dynamische Materialien, bei denen interne Umstrukturierungen, Defekte und metastabile Übergänge eine wichtige Rolle spielen.
Wissenschaftlicher Ansprechpartner:
Dr. Thomas Götsch, goetsch@fhi-berlin.mpg.de
Originalpublikation:
https://www.nature.com/articles/s41929-025-01449-9
Weitere Informationen:
https://www.fhi.mpg.de/2192935/2026-01-16_Catalyst-selectivity-as-balancing-act
Ähnliche Pressemitteilungen im idw