Auf frischer Tat ertappt
Auf den Punkt gebracht
• Beim Diebstahl erwischt: Ein Forschungsteam hat sichtbar gemacht, wie die molekulare Kopiermaschine des Influenza-Virus, FluPol genannt, mit der menschlichen Kopiermaschinerie wechselwirkt, um die Kappe der Wirts-RNA zu stehlen.
• Molekularer Mechanismus entschlüsselt: Den Vorgang des Diebstahls in atomarer Auflösung direkt beobachten zu können, schließt eine Wissenslücke, wie sich einer der häufigsten viralen Krankheitserreger des Menschen vermehrt.
• Aktivität der viralen Kopiermaschine beeinflussbar: Wenn Bereiche der viralen Kopiermaschine verändert werden, die mit der Wirts-Kopiermaschine wechselwirken, ist FluPol in lebenden Zellen weniger aktiv. Dies könnte ein neues Ziel für antivirale Medikamente sein.
Die Erkältungssaison ist in vollem Gange, der Hals kratzt, die Nase läuft, man fühlt sich krank – und hofft, dass es keine Grippe ist. Das Influenza-Virus ist nach wie vor eine Bedrohung für unsere Gesundheit. Es löst saisonale Epidemien aus, seltener auch schwerwiegende weltweite Pandemien. Verfügbare antivirale Medikamente sind oft weniger wirksam als erhofft, da das Influenza-Virus extrem schnell mutiert, um deren Wirkung zu entgehen. Auch Impfstoffe müssen wegen der hohen Wandlungsfähigkeit des Virus jedes Jahr angepasst werden.
Doch Influenza-Viren haben eine „Achillesferse“, die sich für Therapien ausnutzen lässt: ihre Kopiermaschine, die einen der wichtigsten Schritte für die Virusvermehrung ausführt. Forschende aus Göttingen haben nun in Kooperation mit Kolleg*innen an Forschungseinrichtungen in Frankreich sichtbar gemacht, wie das Influenza-Virus mit der Kopiermaschine des Wirts wechselwirkt, um die Kappe der Wirts-RNA zu stehlen und für sich selbst zu nutzen.
Molekularer Diebstahl
Influenza-Viren sind RNA-Viren und besitzen ein Genom aus einzelsträngiger RNA. Wie andere Viren auch, schmuggelt das Influenza-Virus sein Erbgut in die Wirtszelle und nutzt deren molekulares Repertoire, um neue Viruspartikel zu produzieren. Dabei hebelt das Influenza-Virus die Schutzvorkehrungen der Wirtszelle effektiv aus. Durch den Diebstahl der RNA-Kappe des Wirts fördert das Influenza-Virus nicht nur seine eigene Replikation, sondern umgeht auch eine der Schutzmaßnahmen der Wirtszelle.
Die molekularen „Kopiermaschinen“ von Wirtszelle und Virus, beides sogenannte Polymerasen, spielen dabei eine Schlüsselrolle. In der Wirtszelle haben menschliche Polymerasen die Aufgabe, die genomische DNA in prä-mRNA umzuschreiben. Die prä-mRNA wird zu Beginn ihrer Herstellung an ihrem Anfang mit einer chemischen Struktur markiert, die als Kappe bezeichnet wird. Die Kappe ist unbedingt erforderlich, damit die reife mRNA als Bauplan dienen kann, um Proteine zu produzieren. Darüber hinaus markiert die Kappe die RNA als zelleigenes Molekül und damit als harmlos. Fehlt die schützende Kappe, erkennt das Immunsystem die RNA als fremd und potenziell schädlich – und löst eine antivirale Reaktion aus.
„Die meisten Viren haben eine eigene Maschinerie, um die Kappe anzubringen und so ihre mRNA vor dem Immunsystem des Wirts zu verbergen. Dem Grippe-Virus aber fehlt diese Fähigkeit. Stattdessen hat seine Polymerase einen einzigartigen Mechanismus zum Entreißen der Kappe der Wirts-mRNA entwickelt. Im Rahmen einer internationalen Zusammenarbeit ist es uns nun gelungen, diesen Prozess im molekularen Detail sichtbar zu machen“, sagt Patrick Cramer aus der Max-Planck-Gesellschaft und Letztautor der Studie, die jetzt im Fachmagazin Nature erschienen ist.
Geschickt getarnt
Seit vielen Jahren ist bekannt, dass die Kopiermaschine des Influenza-Virus, FluPol genannt, auf Beutezug geht, um die virale mRNA vor dem Immunsystem der Wirtszelle zu verstecken. Sie stiehlt die Kappe von der Wirts-RNA und markiert damit seine eigene. Die Wirtszelle erkennt die virale mRNA nun ebenfalls als Vorlage für die Baupläne von Proteinen und beginnt, alle Proteine herzustellen, die das Virus zu seiner Vermehrung benötigt. Bereits bekannt ist, dass FluPol bei diesem Diebstahl mit der Kopiermaschinerie des Wirts wechselwirkt. Der genaue Mechanismus jedoch war bislang unklar.
„Wie genau das Kap-Stehlen funktioniert, ist seit Jahren ein Rätsel in der Influenza-Forschung“, sagt Stephen Cusack vom Europäisches Laboratorium für Molekularbiologie (EMBL) in Grenoble, der Pionierarbeit in der Strukturanalyse von FluPol geleistet hat. „Dazu muss FluPol in den normalen Prozess der RNA-Synthese des Wirts eingreifen und zum Vorteil des Virus und zum Nachteil der Zelle verändern. Um dieses Rätsel zu lösen, haben wir uns mit Patrick Cramer zusammengetan, einem weltweit führenden Experten für zelluläre Polymerasen.“
Ein interdisziplinäres Team um Patrick Cramer, Stephen Cusack und Nadia Naffakh am Institut Pasteur in Paris haben jetzt erstmals im molekularen Detail schrittweise sichtbar gemacht, wie dieser Diebstahl abläuft. In biochemischen Experimenten gelang es den Forschenden, den Prozess im Reagenzglas nachzustellen. Dazu stoppten sie den Prozess zu verschiedenen Zeitpunkten und verwendeten Kryo-Elektronenmikroskopie, um die Strukturen und Wechselwirkungen der beteiligten Proteine in 3D und mit nahezu atomarer Auflösung sichtbar zu machen.
Diebstahl in drei Etappen
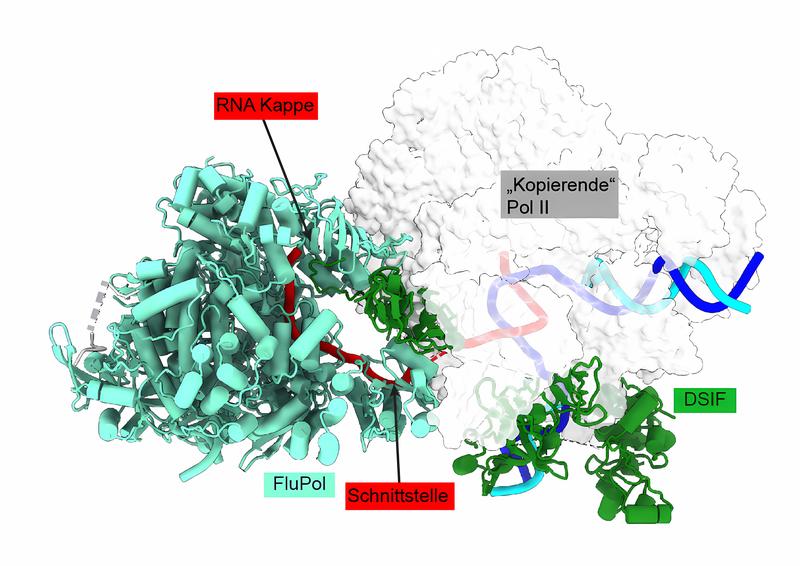
„Wir haben herausgefunden, dass sich der molekulare Diebstahl in drei Hauptschritte unterteilen lässt“, berichtet Alexander Rotsch, ehemaliger Doktorand in der Abteilung Molekulare Biologie am Max-Planck-Institut (MPI) für Multidisziplinäre Naturwissenschaften und einer der Hauptautor*innen der Arbeit. Im ersten Schritt bindet FluPol an die menschliche Kopiermaschine, RNA-Polymerase oder Pol II genannt, während diese eine Wirts-RNA herstellt. Dies geschieht unmittelbar, nachdem die Kappe hinzugefügt wurde. In diesem Schritt verändern beide Polymerasen ihre Strukturen, sodass eine enge Verbindung entsteht. Als Nächstes schneidet FluPol ein kleines Stück der Wirts-RNA ab, das die Kappe enthält. Im letzten Schritt verlängert FluPol die entwendete RNA unter Verwendung der viralen genomischen RNA als Vorlage. „Die fertige virale mRNA sieht genauso aus wie eine Wirts-mRNA, ist voll funktionsfähig, um virale Proteine zu produzieren, und ist dennoch für das Immunsystem des Wirts unsichtbar“, so Rotsch.
Wie die Forschenden weiter zeigen konnten, ist für den Diebstahl neben den beiden Kopiermaschinen noch ein dritter Partner entscheidend: das Helferprotein DSIF, das die Aktivität der Pol II reguliert. „Die Möglichkeit, die genaue Abfolge und die Wechselwirkungen der Proteinpartner im molekularen Detail zu beobachten, schließt eine große Lücke in unserem Verständnis darüber, wie sich einer der häufigsten viralen Erreger in menschlichen Zellen vermehren kann“, betont Christian Dienemann, Projektgruppenleiter in der Abteilung Molekulare Biologie und Leiter der Facility für Kryo-Elektronenmikroskopie am MPI.
FluPol hemmen, um Influenza-Viren zu bekämpfen
Dass die FluPol für die Vermehrung des Virus unentbehrlich ist, macht es auch zu dessen „Achillesferse“. Medikamente zur Behandlung der Grippe zielen daher unter anderem darauf ab, die Fähigkeit von FluPol, die Kappe der Wirts-RNA zu stehlen, zu blockieren. „Wir haben festgestellt, dass die FluPol auch weniger aktiv ist, wenn wir die Stellen verändern, an denen sie mit dem menschlichen Pol II-DSIF-Komplex bindet. Diesen hemmenden Effekt konnten wir auch in lebenden Zellen nachweisen“, berichtet Maud Dupont, ebenfalls Hauptautorin der Studie und Doktorandin im Labor von Nadia Naffakh am Institut Pasteur. Die Wechselwirkungen könnten ein neues Ziel für Medikamente sein, um das Influenza-Virus in Schach zu halten.
Wissenschaftlicher Ansprechpartner:
Dr. Christian Dienemann
Projektgruppenleiter, Abteilung Molekularbiologie
Leiter der Facility für Kryo-Elektronenmikroskopie
Max-Planck-Institut für Multidisziplinäre Naturwissenschaften, Göttingen
E-Mail: christian.dienemann@mpinat.mpg.de
Tel.: +49 551 201-2819
Originalpublikation:
Rotsch, A.H.; Li, D.; Dupont, M.; Krischuns, T.; Neef, U.; Oberthuer, C.; Stelfox, A.; Lukarska, M.; Fianu, I.; Lidschreiber, M.; Naffakh, N.; Dienemann, C.; Cusack, S.; & Cramer, P.: Mechanism of co-transcriptional cap-snatching by influenza polymerase. Nature (4. März 2026).
https://doi.org/10.1038/s41586-026-10189-0
Weitere Informationen:
https://www.mpinat.mpg.de/5179213/pr_2604 – Original-Pressemitteilung
https://www.mpinat.mpg.de/de/cramer – Abteilung Molekularbiologie, Max-Planck-Institut für Multidisziplinäre Naturwissenschaften, Göttingen
Ähnliche Pressemitteilungen im idw