Neues Biomaterial fördert die Regeneration von Gewebe
Viele Erkrankungen, von chronischen Wunden etwa infolge einer Diabetes-Erkrankung bis hin zu Herz-Kreislauf-Erkrankungen, entstehen, weil geschädigtes Gewebe im Körper nicht mehr stabil aufgebaut werden kann. Statt zu heilen, wird die körpereigene Struktur durch ein Ungleichgewicht in den körpereigenen Regulationsmechanismen zunehmend abgebaut. Ein Forschungsteam der Universität des Saarlandes hat nun gemeinsam mit Partnern ein Gel entwickelt, das diesen Prozess stoppen und so die Heilung beschleunigen kann.Die interdisziplinäre Studie verbindet materialwissenschaftliche, vorklinische und klinische Forschung und wurde jüngst im hochrangigen Fachjournal Bioactive Materials veröffentlicht.
Die Abläufe im menschlichen Körper sind aufeinander abgestimmt wie in einem unglaublich komplexen Uhrwerk – nur statt mit einigen Dutzend oder Hunderten Zahnrädchen mit Billionen Zellen, Zellbestandteilen und Stoffen, die sich gegenseitig beeinflussen. So sorgt zum Beispiel ein Botenstoff dafür, dass vermehrt Bestandteile hergestellt werden, die die Heilung von Gewebe beschleunigen. Kommt es nun aufgrund einer Krankheit dazu, dass ein solcher Stoff nicht in ausreichendem Maße an eine Stelle gebracht wird, wo defektes Gewebe erneuert werden muss, können schwerwiegende Folgen eintreten. Das ist zum Beispiel bei chronischen Wunden bei Diabetikern der Fall, die an „offenen Beinen“ leiden, oder auch bei bestimmten Herz-Kreislauf-Erkrankungen und bei Komplikationen nach zahnmedizinischen Restaurationen. Hierbei ist das körpereigene Gleichgewicht der Regulationsmechanismen aus den Fugen geraten. Statt das Gewebe wieder aufzubauen und eine Wunde zu schließen, wird es stattdessen weiter abgebaut – oft mit fatalen Folgen.
Wissenschaftlerinnen und Wissenschaftlern um Sandra Rother ist nun ein wichtiger Schritt gelungen, um dieses Ungleichgewicht wieder in Balance zu bringen. „Im Zentrum unseres Ansatzes steht ein neuartiges Hydrogel, das natürliche Bestandteile des Gewebes nachahmt“, erklärt die Juniorprofessorin für Molekulare Signalverarbeitung an der Universität des Saarlandes den Kern einer nun veröffentlichten Studie, die unter ihrer Federführung im hochrangigen Fachjournal Bioactive Materials veröffentlicht wurde. Dabei nutzte ihr interdisziplinäres Team sogenannte Glykosaminoglykane (GAGs), lange Zuckerketten, die natürlicherweise im Gewebe vorkommen und dort helfen, wichtige Botenstoffe zu binden und zu stabilisieren.
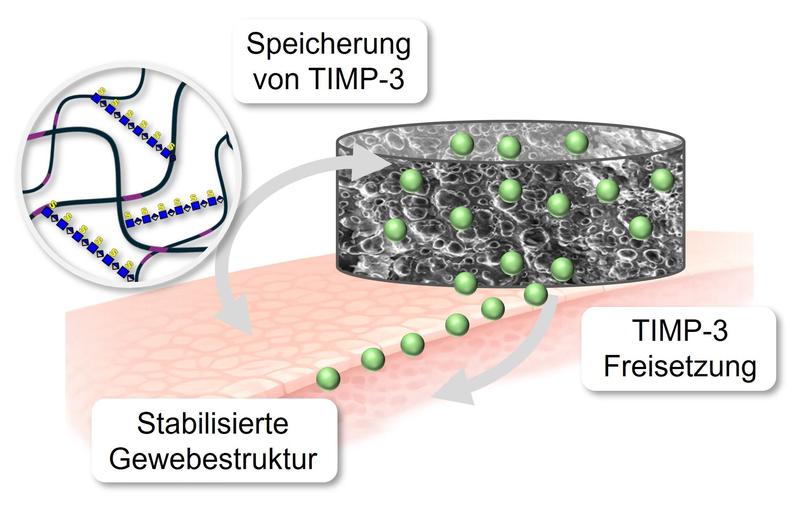
„Durch ihre Integration in das Hydrogel kann ein körpereigener Schutzfaktor gezielt lokal bereitgestellt werden, der so genannte Tissue Inhibitor of Metalloproteinases-3, kurz TIMP-3“, so die Wissenschaftlerin. Dieses Protein wirkt wie eine natürliche Bremse für Enzyme, die Gewebe abbauen, deren Kontrolle häufig gestört ist, wenn sie durch Krankheiten wie Diabetes beeinflusst werden. „Das von uns neu entwickelte Material speichert TIMP-3 und gibt es über längere Zeit hinweg kontrolliert ab. So kann der Schutzmechanismus direkt im betroffenen Gewebe wirken, anstatt im gesamten Körper verteilt zu werden“, führt Sandra Rother aus. „In experimentellen Modellen konnten wir so eine Stabilisierung der Gewebestruktur nachweisen, eine reduzierte Entzündungsreaktion sowie eine gezielte Eindämmung krankhafter Abbauprozesse.“ Die interdisziplinäre Studie, an der neben der theoretischen Medizin auch die klinische Medizin des Universitätsklinikums eingebunden war, das Leibniz-Institut für Neue Materialien, die TU Dresden sowie Einrichtungen in Jena, könnte somit einen neuen Weg für die Entwicklung von Therapien solcher Begleiterscheinungen von Krankheiten wie Diabetes aufzeigen.
Wissenschaftlicher Ansprechpartner:
Jun.-Prof. Dr. Sandra Rother
Tel.: (06841) 1616208
E-Mail: sandra.rother@uks.eu
Originalpublikation:
Junker F, Rupf S, Schindler PM, Wilden C, Hohl M, Ruiz-Gómez G, Pisabarro MT, Wrublewsky S, Bickelmann C, Berhorst C, Alansary D, Wieland B, Bischoff M, Lee PS, Moeller S, Berg A, Dancker TA, Lauterbach MA, Ganse B, Roma LP, Steudter T, Metzger W, Tschernig T, Ampofo E, Laschke MW, Hannig M, Rother S. Glycosaminoglycan-functionalized hydrogels for sustained delivery of tissue inhibitor of metalloproteinase-3 mediating matrix metalloprotease inhibition and extracellular matrix stabilization. Bioact Mater. 2026 Feb 12;61:172-193. doi: 10.1016/j.bioactmat.2026.02.010. PMID: 41732672; PMCID: PMC12924898.
Ähnliche Pressemitteilungen im idw