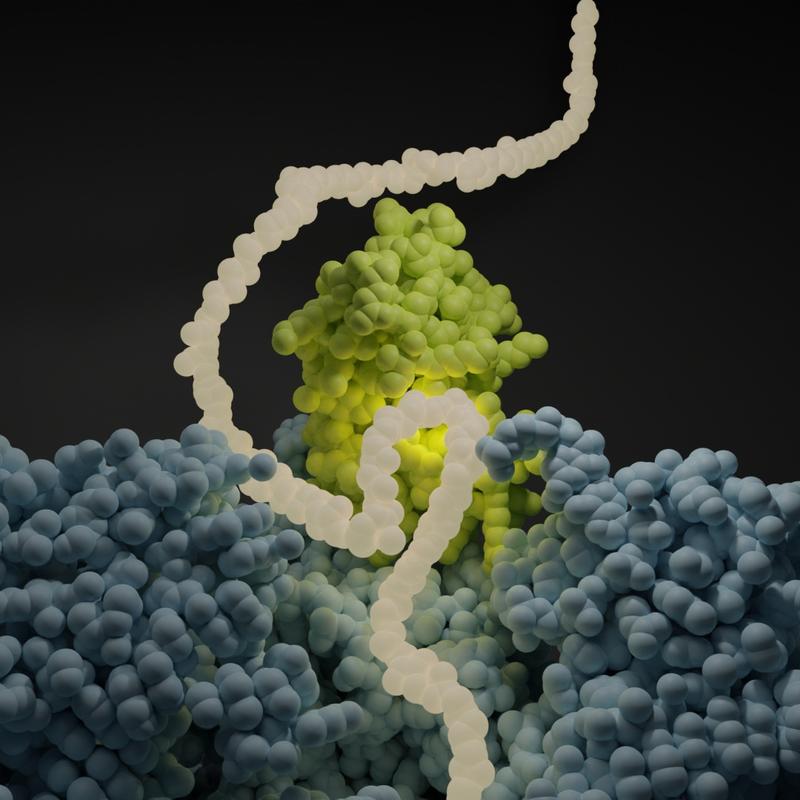
Neue Erkenntnisse zu den ersten Schritten der Proteinsynthese
In der frühesten Phase der Herstellung menschlicher Proteine erfüllt der Proteinkomplex NAC eine wesentliche Aufgabe, indem er die ersten Schritte der Faltung der Proteine in ihre korrekten dreidimensionalen Strukturen einleitet. Das hat ein internationales Forschungsteam unter Federführung von Wissenschaftlern des Zentrums für Molekulare Biologie der Universität Heidelberg herausgefunden. Danach bindet der NAC-Komplex an die gerade durch das Ribosom gebildeten Proteinbausteine, die Aminosäureketten, und initiiert ihre für die Funktionalität der Proteine essentielle Faltung.
Pressemitteilung
Heidelberg, 23. März 2026
Neue Erkenntnisse zu den ersten Schritten der Proteinsynthese
Internationales Forschungsteam unter Heidelberger Federführung untersucht Rolle des NAC-Komplexes im essentiellen Prozess der Proteinfaltung
In der frühesten Phase der Herstellung menschlicher Proteine erfüllt der Proteinkomplex NAC eine wesentliche Aufgabe, indem er die ersten Schritte der Faltung der Proteine in ihre korrekten dreidimensionalen Strukturen einleitet. Das hat ein internationales Forschungsteam unter Federführung von Wissenschaftlern des Zentrums für Molekulare Biologie der Universität Heidelberg herausgefunden. Danach bindet der NAC-Komplex an die gerade durch das Ribosom gebildeten Proteinbausteine, die Aminosäureketten, und initiiert ihre für die Funktionalität der Proteine essentielle Faltung. Die Forschungsergebnisse liefern nach Angaben der Wissenschaftler nicht nur neue Erkenntnisse zur Proteinsynthese, sondern auch Einblicke in zelluläre Strategien zur Vermeidung von Fehlfaltungen, die zu schweren Krankheiten führen können.
Der Proteinkomplex NAC – kurz für Nascent Polypeptide-Associated Complex – kommt in allen Eukaryoten vor und übernimmt auch in menschlichen Zellen überlebenswichtige Aufgaben im Zusammenhang mit der Proteinsynthese. Dazu bindet NAC an die Proteinfabrik der Zellen, das Ribosom, wo er mithilfe von Enzymen und anderen molekularen Faktoren die verschiedenen Schritte der Herstellung von Proteinen koordiniert. Nicht bekannt war nach Angaben des Heidelberger Molekularbiologen Prof. Dr. Bernd Bukau bislang, inwiefern der NAC-Komplex auch direkt eine Rolle bei der Proteinfaltung spielt. Während dieses Faltungsprozesses nehmen die ursprünglich linearen Aminosäureketten ihre für jedes Protein spezifische dreidimensionale Struktur an. Erst danach sind die Proteine funktionstüchtig. Fehler bei der Faltung werden in Zusammenhang mit vielen Krankheiten gebracht, einschließlich neurodegenerativen Erkrankungen wie Alzheimer, Parkinson oder Chorea Huntington.
Das internationale Forschungsteam hat nun herausgefunden, dass der Proteinkomplex NAC bereits in die sehr frühen Stadien der Proteinfaltung eingreift, das heißt sobald die im Ribosom hergestellten Aminosäureketten den ribosomalen Tunnel verlassen. In ihren Untersuchungen stellten die Wissenschaftler fest, dass NAC an einen Großteil aller in einer menschlichen Zelle hergestellten, naszierenden Proteine bindet, also bereits während ihrer noch laufenden Synthese durch das Ribosom. In biophysikalischen Analysen mit Einzelmolekülen konnten sie nachweisen, dass der NAC-Komplex dadurch die korrekte Faltung von Proteinen bewirkt. „Gleichzeitig verhindert NAC damit, dass unvollständige Zwischenprodukte zu Fehlfaltungen führen“, erläutert Prof. Bukau, der am Zentrum für Molekulare Biologie der Universität Heidelberg (ZMBH) die Forschungsgruppe „Biogenese und Qualitätskontrolle von Proteinen“ leitet.
Mithilfe von Kryo-Elektronen-Mikroskopie konnte das internationale Forschungsteam außerdem zeigen, wie der NAC-Komplex an die gerade entstandenen Aminosäureketten bindet. NAC besitzt eine dem ribosomalen Tunnel zugewandte Bindestelle, die auf bestimmte Bereiche in den naszierenden Proteinen ausgelegt ist. Eine im Zuge der Experimente künstlich erzeugte Variante des Proteinkomplexes, der diese Bindestelle fehlt, konnte die Faltungsfunktion von NAC nicht mehr erfüllen. Das Team hat auch herausgefunden, dass NAC dynamisch auf die jeweilige Beschaffenheit der naszierenden Proteine reagiert und seine Position am Tunnelausgang des Ribosoms verändert. Dadurch kann der NAC-Komplex seine Rolle als Faltungshelfer an die Bedürfnisse des Faltungsvorgangs anpassen. „In der Forschung ist schon lange bekannt, dass der NAC-Komplex auf vielfältige Art und Weise in die verschiedenen Prozesse der Proteinsynthese eingreift und dabei als molekulare Schaltzentrale eine ganz bedeutende Rolle spielt. Mit unseren Ergebnissen können wir dem noch unvollständigen Bild ein weiteres Puzzleteil hinzufügen“, so Dr. Günter Kramer, Leiter der an dieser Studie beteiligten ZMBH-Gruppe „Kotranslationale Proteinreifung“.
Die Forschungsarbeiten wurden im Rahmen des ERC Synergy-Konsortiums „Mechanisms of co-translational assembly of multi-protein complexes“ durchgeführt. Dieses mit Mitteln des Europäischen Forschungsrates (ERC) geförderte Verbundvorhaben wird von Prof. Bukau an der Universität Heidelberg koordiniert. Beteiligt sind daran auch die Teams von Prof. Dr. Sander Tans vom AMOLF-Forschungsinstitut für die Physik funktioneller komplexer Materie in Amsterdam (Niederlande) und von Prof. Dr. Nenad Ban, der an der Eidgenössischen Technischen Hochschule Zürich (Schweiz) forscht. Zu den aktuellen Arbeiten hat außerdem die Forschungsgruppe von Prof. Dr. Shu-ou Shan am California Institute of Technology in Pasadena / Kalifornien (USA) beigetragen. Gefördert wurden die Arbeiten neben dem ERC auch von der Deutschen Forschungsgemeinschaft, den National Institutes of Health und der National Science Foundation (USA) sowie dem Schweizerischen Nationalfonds. Die Forschungsergebnisse sind in „Molecular Cell“ erschienen.
Kontakt:
Universität Heidelberg
Kommunikation und Marketing
Pressestelle, Telefon (06221) 54-2311
presse@rektorat.uni-heidelberg.de
Wissenschaftlicher Ansprechpartner:
Prof. Dr. Bernd Bukau
Zentrum für Molekulare Biologie der Universität Heidelberg
Telefon (06221) 54-6795
bukau@zmbh.uni-heidelberg.de
Originalpublikation:
J. Santos, M. Günnigmann, R. J. Gora, M. Iljina, M. Predin, I. E. Kotan, P. De, D. Choudhary, J. Jang, F. Tippmann, C. Hins, N. Ban, S. J. Tans, S. Shan, G. Kramer, and B. Bukau: NAC promotes co-translational protein folding at the ribosomal tunnel exit. Molecular Cell (23 March 2026), https://doi.org/10.1016/j.molcel.2026.02.022
Weitere Informationen:
https://www.zmbh.uni-heidelberg.de/Bukau/default.shtml – Bernd Bukau
https://www.zmbh.uni-heidelberg.de/kramer/default.shtml – Günter Kramer
Ähnliche Pressemitteilungen im idw