Logistikmeister in der Zelle: Forscher entschlüsseln das „Navi “ für mRNA
Biologie: Breakthrough-Veröffentlichung in Nucleic Acids Research
Wie in einer riesigen Fabrik müssen auch in lebenden Zellen Bauteile exakt zum richtigen Zeitpunkt am passenden Ort ankommen. Ein Forschungsteam unter der Leitung der Heinrich-Heine-Universität Düsseldorf (HHU) hat im Pilz Ustilago maydis untersucht, wie das Transportprotein Rrm4 als hochpräziser Logistiker fungiert. Die Arbeit wurde aufgrund ihrer Bedeutung als „Breakthrough-Manuskript“ in der renommierten Fachzeitschrift Nucleic Acids Research (NAR) veröffentlicht.
Im Inneren jeder Zelle liegt der Bauplan des Lebens – die DNA – gut geschützt im Zellkern. Um daraus Proteine – die Werkzeuge der Zelle – herzustellen, wird eine Kopie des Bauplans erstellt: die sogenannte „Messenger-RNA“ (kurz mRNA). Diese muss anschließend dorthin gelangen, wo die Zelle sie braucht, etwa zu den Proteinfabriken.
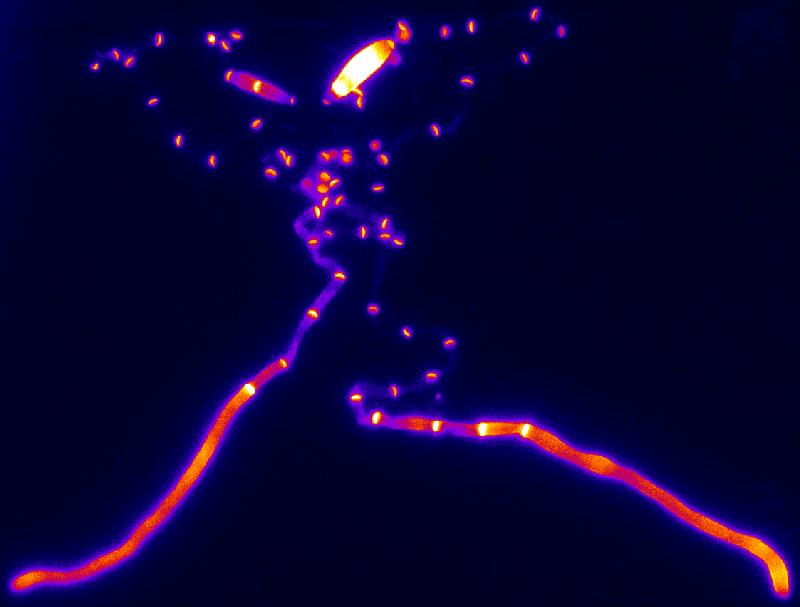
Bei Ustilago maydis, der in Mais die Pilzkrankheit „Maisbeulenbrand“ auslöst, müssen die mRNAs über weite Strecken bis zu den äußersten Spitzen seiner fadenförmigen Ausläufer (die „Hyphen“) transportiert werden. Damit spielen Transportprozesse und ihre Steuerung für das Funktionieren der Zellen eine zentrale Rolle. Um an entfernte Orte zu gelangen, wird ein aktiver Expresstransportdienst benötigt.
Das Transportprotein Rrm4 übernimmt in Ustilago maydis diese Logistikaufgabe. Es besitzt drei spezialisierte „Greifarme“ (sogenannte RRMs; RNA-Recognition Motifs), mit denen es die mRNA greift und auf membranumschlossene Organellen (Endosomen) verlädt. Diese fungieren wie Frachtwaggons, die entlang der Mikrotubuli wie auf Schienen durch die Zelle rasen.
Doch wie erkennt das Transportprotein, welche mRNAs es greifen muss? Mithilfe der hochpräzisen iCLIP2-Methode zeigten die Forschenden um Prof. Dr. Michael Feldbrügge vom HHU-Institut für Mikrobiologie, dass die mRNA spezifische „Zipcodes“ (quasi Postleitzahlen) besitzt. Nur wenn der Greifarm des Proteins genau in diesen Zipcode passt, wird das Paket korrekt verladen und – was ebenso wichtig ist – unterwegs stabil gehalten.
„Diesen Prozess im Detail zu verstehen, war nur durch eine enge Verzahnung der Disziplinen möglich. Während die experimentellen Biologen im Labor in Düsseldorf die Pilze untersuchten und Mutationen analysierten, bewältigten Computerbiologen aus Würzburg die enorme Datenkomplexität. Erst durch die computergestützte Auswertung konnten die Millionen von Bindungspunkten zwischen Protein und RNA entschlüsselt und die funktionell wichtigen Bindestellen identifiziert werden“, erläutert Prof. Feldbrügge, Korrespondenzautor der in NAR erschienenen Studie, das Zusammenspiel der verschiedenen Kooperationspartner. Er ergänzt: „Wir entschlüsselten so die Funktion des Proteins Rrm4 in einer bisher nicht erreichten hohen Auflösung. Unser Ansatz kann auch für eine Vielzahl anderer Proteine dienen.“
Die Forschenden fanden, dass jeder der drei Greifarme eine unterschiedliche Aufgabe bei der Erkennung der mRNA hat. Die Bindung entscheidet nicht nur über den Transport, sondern auch darüber, wie lange eine mRNA haltbar bleibt, bevor sie abgebaut wird. Durch gezieltes „Ausschalten“ einzelner Greifarme zeigte sich, dass ohne eine exakte Bindung die gesamte Logistik der Zelle zusammenbricht – der Pilz kann nicht mehr normal wachsen.
Ein besonderer Fokus der Arbeit lag auf mRNAs, die für die Mitochondrien (die Kraftwerke der Zelle) bestimmt sind. Sie sind auf eine ständige Versorgung mit mRNAs angewiesen. Den Forschenden gelang es nun zu verstehen, wie Kern, Endosomen und Mitochondrien miteinander kommunizieren.
Das intrazelluläre Networking ist eine Kernfragestellung des Düsseldorfer Sonderforschungsbereichs SFB 1535 MibiNet, in dessen Rahmen die Untersuchungen durchgeführt wurden. „Wir haben nun verstanden, wie die Zelle durch den gezielten Transport von mRNA sicherstellt, dass die Energieversorgung und die Kommunikation zwischen den verschiedenen Zellbereichen reibungslos funktionieren“, so Prof. Feldbrügge, Sprecher des SFB.
Diese Ergebnisse der Grundlagenforschung an einem Pilz reichen auch weit in die moderne Medizin hinein. Prof. Feldbrügge zu möglichen weiterführenden Perspektiven: „Wenn klar ist, wie mRNA transportiert, erkannt und stabilisiert wird, können auf der Basis beispielsweise mRNA-Impfstoffe – die aus der Coronapandemie bekannt sind – weiterentwickelt, präziser und wirksamer gemacht werden.“
Die Arbeit wurde von der Zeitschrift NAR als sogenanntes Breakthrough-Manuskript ausgezeichnet. Dies zeigt die besondere Bedeutung der Studie: Nur die besten zwei Prozent der eingereichten Arbeiten erhalten eine solche Bewertung.
Originalpublikation:
Nina Kim Stoffel, Srimeenakshi Sankaranarayanan, Kira Müntjes, Anke Busch, Julian König, Kathi Zarnack, Michael Feldbrügge; Dissecting the RNA-binding capacity of the multi-RRM protein Rrm4 essential for endosomal mRNA transport; Nucleic Acids Research, 2026, 54, gkag210
DOI: 10.1093/nar/gkag210
Weitere Informationen:
https://www.sfb1535.hhu.de/mibinet
Ähnliche Pressemitteilungen im idw